W. HASIBEDER
INTUBATION KRITISCH KRANKER – ETOMIDATE VERSUS KETAMIN
In einer prospektiven, randomisierten Studie (14 Notaufnahmen und Intensivstationen in den USA) wurden kritisch kranke Patient:innen mit Notwendigkeit für eine tracheale Intubation in 2 Gruppen randomisiert. 1176 Patient:innen wurden mit Ketamin anästhesiert; 1189 mit Etomidate. Der primäre Outcomeparameter war der Tod bis zum 28. Tag. Als sekundäre Outcomeparameter wurden ein Kreislaufkollaps während der Intubation (RRsys < 65mmHg) oder die Notwendigkeit zur Steigerung einer Vasopressortherapie oder eine Herzkreislaufstillstand um die Intubation monitiert.
Die Intubationsdosis in der Ketamingruppe lag zwischen 1-2mg/kg Körpergewicht; in der Etomidategruppe zwischen 0,2 und 0,3mg/kg Körpergewicht. Das Medianalter der Patient:innen war 60 Jahre; fast 50% litten an einer Sepsis oder einen septischen Schock. 56% wurden auf der Notaufnahme intubiert, der Rest auf einer Intensivstation.
Die Autoren berichten keine Unterschiede in der 28-Tage Mortalität zwischen den Gruppen (Ketamin Gruppe 32,2%; Etomidate Gruppe 32,4%). Ein kardiovaskulärer Kollaps während der Intubation war unter Ketamin häufiger (22,1%) verglichen mit Etomidate (17%). Hier fand sich der größte Unterschied bei Patient:innen mit Sepsis oder septischen Schock (Ketamin 30,6% kardiovaskuläre Kollaps Ereignisse; Etomidate 2,9%). Auch die mediane Zeit bis zur erfolgreichen Intubation war unter Etomidate mit 103 Sekunden (IQR: 80-134 Sekunden) kürzer als in der Ketamingruppe (Median: 112 Sekunden; IQR: 86-155).
FAZIT für die Praxis: Etomidate ist ein Imidazol-Derivat mit sedativen und hypnotischen Eigenschaften, dass über ?-Aminobuttersäure Rezeptoren am Gehirn wirkt. Außerdem kann Etomidate das Enzym 11ß-Hydroxylase der Nebennierenrinde reversibel hemmen und damit die Cortisol Synthese bis zu 72 Stunden unterdrücken. Diese Eigenschaft wurde in früheren Untersuchungen als schwerer Nachteil des Medikaments angesehen und eine Etomidate induzierte Nebenniereninsuffizienz mit erhöhtem Risiko für kardiovaskulärer Verschlechterung und Tod angesehen. Im Gegensatz dazu hat Ketamin keinerlei Einfluss auf die Cortisol Produktion. Die Hypnose wird über N-Methyl-D-Aspartat Rezeptoren mediiert und Ketamin steigert den Sympathikotonus, was vor allem bei kritisch kranken Patient:innen als möglicher Vorteil bei der Einleitung einer Anästhesie gesehen wird. Observationsstudie weisen allerdings auch auf einen vasodilatorischen Effekt von Ketamin mit Auftreten teils schwerer Hypotension, Arrhythmien und möglichen Herzkreislaufstillstand hin. Die vorliegende „Entweder Oder“ Studie zeigt keinerlei Unterschiede in der 28-Tage Mortalität zwischen den beiden Hypnotika. Bei der Einleitung zeigte Etomidate eine bessere hämodynamische Stabilität der Patient:innen im Vergleich mit Ketamin. Als Leser darf man nicht außer Acht lassen, dass die Einleitung der Hypnose zur Intubation nicht den üblichen klinischen Vorgehensweisen entspricht. Meist werden Medikamente in Kombinationen verwendet um Nebenwirkungen einer einzelnen Substanz möglichst gering zu halten! Wir leiten „schlechte“ Patient:innen meist mit einer Kombination aus Opiat (z.B. Fentanyl 0,1mg), Ketanaest S (12,5-25mg) und Etomidate (10-12mg) ein. Mit dieser Kombination ist größtmögliche hämodynamische Stabilität garantiert. Nach dem Einleiten wird die Anästhesie entsprechend den physiologischen und chirurgischen Erfordernissen adaptiert und fortgeführt.
Literatur:
Casey JD et al. Ketamine or Etomidate for tracheal intubation of critically ill adults. NEJM 2025; doi: 10.1056/NEJMoa2511420
GLUCOCORTICOIDE ALS ADJUVANTE THERAPIE BEI CAP AUSSERHALB DES KRANKENHAUSES
Wir haben mehrfach über die Bedeutung einer adjuvanten Steroidtherapie bei der Behandlung schwerer, vorwiegend bakterieller Pneumonien mit Notwendigkeit einer Hospitalisation, berichtet. Die letzten Guidelines empfehlen eine Therapie mit Steroiden bei schwerer bakterieller CAP auch ohne septischen Schock.
In einer neuen prospektiven, randomisierten Studie aus Kenia wurden Steroide als adjuvante Therapie bei außerhalb des Krankenhauses erworbenen Pneumonien (CAP) verabreicht. Eine orale niedrigdosierte Glucocorticoidtherapie wurde gemeinsam mit einer oralen Penicillin- oder Cephalosporin- Antibiose in Kombination mit einem Macrolid-Antibiotikum verabreicht. Glucocorticoide wurden je nach regionaler Verfügbarkeit in Bioäquivalenzdosierungen gegeben: 6 mg Dexamethason; 160mg Hydrocortison; 30mg Methylprednisolon oder 50mg Prednisolon einmal am Tag.
Das mediane Alter der Patient:innen war 53 Jahre; 15,5% litten an einer HIV-Infektion. Mehr als 1/3 der Patient:innen zeigten bei Beginn der Therapie eine pulsoxymetrisch gemessene arterielle Sättigung < 90% und 10% der Patient:innen waren hypotensiv. 1089 Patient:innen mit CAP erhielten adjuvant Glucocorticoide; 1091 wurden nur antibiotisch behandelt (Standard Care). Der primäre Outcomeparameter war die 30 Tage Mortalität. Sekundäre Outcome Parameter waren Auftreten von Nebenwirkungen im Beobachtungszeitraum. Die Glucocorticoidtherapie wurde für 10 Tage durchgeführt. Steroide wurden abrupt ohne Ausschleichen beendet.
Die 30 Tage Mortalität war in der Standard Care Gruppe signifikant erhöht (26% vs. 22,6%; p<0.02). Die Häufigkeit von Nebenwirkungen war in beiden Gruppen ähnlich, wobei in der Steroidgruppe häufiger Hyperglykämien auftraten.
FAZIT für die Praxis: In einem Editorial zu Studie schreiben Kwizera und Dünser, wie enorm bedeutend Pneumonien als Erkrankung in diesen gesundheitsökonomisch schlecht entwickelten Ländern Afrikas sind. Einer/Eine von 8 hospitalisierten Patient:innen mit CAP ist kritisch krank. Bei fehlenden Intensivresourcen sterben fast 21% der Betroffenen innerhalb von 7 Tagen. Der Mortalitätsunterschied von 3,4% zwischen Steroid- und Standard Care Gruppe in der SONIA-Studie ist daher als wichtiger Schritt zur Verminderung der Erkrankungsfolgen zu betrachten. Für uns Ärzt:innen, die wir ein einem medizinischen „Schlaraffenland“ leben und arbeiten dürfen bestätigt die Studie die Wichtigkeit eine adjuvanten Steroidtherapie bei schweren bakteriellen CAP zu beginnen!
Literatur:
Lucinde RK, et al. A pragmatic trial of glucocorticoids for community-acquired pneumonia. NEJM 2025; doi: 10.1056/NEJMoa2507100
DIE VERWENDUNG DER KAPILLÄREN FÜLLUNGSZEIT ZUR STEUERUNG DER FRÜHEN RESUSCITATION IM SEPTISCHEN SCHOCK – DIE ANDROMEDA-2 STUDIE
Laktatwerte im septischen Schock können aus unterschiedlichen Gründen erhöht sein und sind nur bedingt als Verlaufsparameter des Erfolgs der hämodynamischen Resuscitation zu verwerten. Bereits 2019 haben Hernandez et al. gezeigt, dass eine Steuerung der hämodynamischen Resuscitation nach kapillärer Füllungszeit (CRFT) einige Outcomeparameter von Patient:innen im septischen Schock verbessert.
In einer neuen Studie mit 1500 inkludierten Patient:innen wurde eine Resuscitation nach CRFT mit einer Standardtherapie (ST) nach Laktat und anderen klinischen Parametern verglichen. In die CRFT Gruppe wurden 720, in die ST-Gruppe 747 Patient:innen randomisiert. Das mittlere Alter der Patient:innen betrug 66 Jahre. Inklusionskriterien waren: Systemische Infektion mit Laktat >2mmol/l und einem MAP von 65mmHg unter NA-Infusion und nach zumindest 1l kristalloider Infusion. Die Patient:innen wurden innerhalb von 4 Stunden nach der Diagnose septischer Schock in die Studie eingeschlossen. Die CRFT wurde bis zur 6. Stunde nach Inklusion in die Studie als Resuscitationsparameter herangezogen.
Die CRFT wurde ventral an einer Fingerbeere gemessen: Ein Glasblättchen wurde bis zum Abblassen der Haut auf die Fingerbeere gedrückt und der Druck wurde für 10 Sekunden gehalten. Anschließend wurde der Druck abrupt beendet und die CRFT gemessen. Als abnormaler Befund wurde eine CRFT > 3 Sekunden gewertet (Abbildung 1). Die CRFT wurde nach jedem Flüssigkeitsbolus nach einem strikten Behandlungsalgorythmus gemessen und weitere Flüssigkeitsboli, bei adäquater myokardialer Pumpfunktion, bis zur Normalisierung der CRFT verabreicht.

Die weitere hämodynamische Therapie in beiden Gruppen bestand neben einer invasiven Überwachung des Blutdrucks, in wiederholten „Leg-Tests“, echokardiographischen Untersuchungen der myokardialen Pumpfunktion und des zentralen Volumenstatus. Alle Patient:innen erhielten Dobutamin in einer niedrigen Dosierung.
Als kombinierter Outcome Parameter wurde die Kombination aus Tod, Notwendigkeit lebenserhaltender Therapien (mechanische Beatmung; Vasopressortherapie; Nierenersatztherapie) und Länge des Krankenhausaufenthalts gewählt.
Die wesentlichen Ergebnisse waren (siehe auch Abbildung 2) :
- Patient:innen mit CRFT Resuscitation hatten gegenüber der ST Gruppe ein signifikant verbessertes Kombinationsoutcome (49% versus 42%; NNT: 15).
- Die Intensivmortalität war mit 17,8% versus 19,1% geringer in der CRFT Gruppe; ebenso war die Dauer lebenserhaltender Therapien und die Spitalsaufenthaltsdauer um 1 Tag kürzer
- Die 28 Tage Mortalität war in beiden Gruppen mit 27% ähnlich
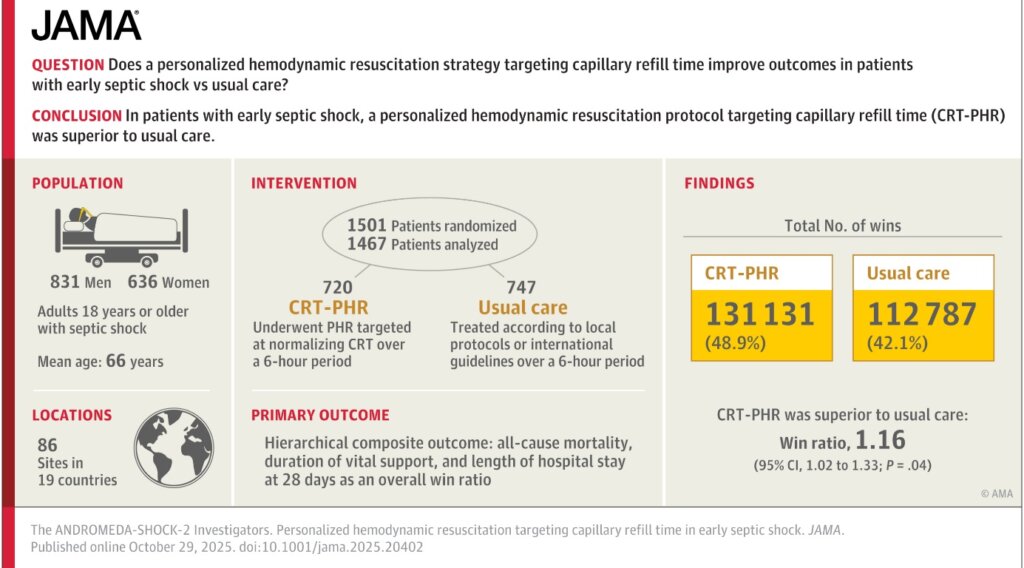
FAZIT für die Praxis: Die CRFT ist bei seit Jahren integraler Bestandteil und eine rasche Normalisierung das Endziel jeder hämodynamischen Resuscitation ob im septischen oder hämorrhagischen Schock an unserer Intensivstation. Selbstverständlich wird die Vorgeschichte der Patient:innen bzw. schwere vorbestehende Herzkreislauferkrankungen in die Bewertung einer gemessenen CRFT miteinbezogen. In der Praxis bedeutet dies, dass z.B. die CRFT bei Patient:innen mit schweren Gefäßerkrankungen zwar gemessen und dokumentiert, aber in Therapieentscheidungen weniger berücksichtigt wird. Natürlich müssen Patient:innen für die Beurteilung der CRFT weitgehend schmerz- und angstfrei sein!
Wir arbeiten in der Resuscitation routinemäßig mit der Pulsdruckvariabilität, bei nicht spontan atmenden Patient:innen, zur Normalisierung des zentralen Blutvolumen und Evaluieren zusätzlich die myokardiale Pumpfunktion mittels Echokardiogaphie. Der „periphere“ Volumenstatus wird anhand der CRFT abgeschätzt. Der Patient/die Patientin gilt als normovoläm, wenn Sie/Er in der Peripherie warm ist und die CRFT sich normalisiert hat.
Literatur:
Hernandez G et al. Personalized hemodynamic resuscitation targeting capillary refill time in early septic shock. The Andromeda-Shock 2 randomized clinical trial. JAMA 2025; 334: 1988-1999
NIEDRIG VERSUS HOCHDOSIERTES NITROGLYCERINE IN DER BEHANDLUNG DES AKUTEN LUNGENÖDEMS
Das akute Lungenödem ist ein lebensbedrohliches Zustandsbild im Rahmen der schweren akuten Herzinsuffizienz. Derzeitige Richtlinien empfehlen die Gabe von iv. Nitroglycerin (NTG) beginnend mit 5µg/min und steigend in 5µg Schritten alle 3-5 Minuten mit dem Ziel den systolischen Blutdruck um 25+5% innerhalb der ersten Behandlungsstunde zu senken.
In dieser retrospektiven, Single Center Kohorten Studie wurden Patient:innen mit akutem Lungenödem im Rahmen einer hypertensiven Krise mit, entweder niedrig dosiertem ( NTG < 100µg/min; n=248) oder hochdosiertem NTG (NTG > 100µg/min; n=193) behandelt. Der primäre Outcomeparameter war die Dauer der Sauerstoffbehandlung zur Erzielung einer arteriellen SO2 > 90%. Sekundäre Outcomeparameter waren das Auftreten von unerwünschten Nebenwirkungen z.B. Verschlechterung der respiratorischen Funktion; Hypotension mit Notwendigkeit zur Vasopressortherapie.
Die Ergebnisse zeigten, dass Patient:innen in der höher dosierten NTG Gruppe rascher von der Sauerstofftherapie entwöhnt waren (2,7h versus 3,3h) und schneller eine systolische Blutdruckreduktion von 25+5% innerhalb von 60 Minuten erreichten. Es gab keine signifikanten Unterschiede im Auftreten unerwünschter Nebenwirkungen zwischen den Gruppen.
FAZIT für die Praxis: Interessant an der Studie ist, dass die Patient:innen in der Hochdosis- NTG Gruppe kränker waren und sich trotzdem ohne gesteigerte Nebenwirkungen rasch mit der Oxygenierung und dem systolischen Blutdruck normalisiert haben. Die Daten zeigen, dass das akute Lungenödem im Rahmen einer hypertensiven Krise mit dekompensierter Herzinsuffizienz aggressiv und sicher mit höher dosierten NTG behandelt werden kann!
Literatur:
Henry K et al. Low versus high dosing strategies of intravenous nitroglycerin for the management of sympathetic crashing acute pulmonary edema. Am J Emerg Med 2025; 98: 41-45
LEBERZIRRHOSE UND DIE BEHANDLUNG VON ASZITES – EIN KURZER ÜBERBLICK AUS DEM JAHR 2025
Obwohl wir Patienten mit Varizenblutungen oder bekannten hochgradigen Varizen schon lange Betablocker verschreiben, war es bisher unklar, ob wir diese Medikamente früher – also sobald bei Patienten mit Leberzirrhose neu aufgetretener Aszites auftritt – einsetzen sollten.
Eine kleine randomisierte Studie aus dem Jahr 2025 mit Carvedilol (vs. keinem Carvedilol) bei Patienten mit Leberzirrhose und neu aufgetretener Aszites (und mit niedrigem Risiko oder ohne Varizen) zeigte, dass Patienten, die Carvedilol erhielten, signifikant weniger Episoden eines hepatorenalen Syndroms, einer spontanen bakteriellen Peritonitis und einer therapierefraktären Aszites aufwiesen (Number Needed to Treat, jeweils 4 bis 7); weniger großvolumige Parazentesen benötigten (NNT 3); und eine geringere Sterblichkeitsrate (9 % vs. 24 %; NNT 6) nach einem Jahr hatten. Zu beachten ist allerdings, dass orthostatische Hypotonie und Hypotonie häufig bei Patienten mit Leberzirrhose auftreten und durch eine Betablocker-Therapie verstärkt werden können.
Eine weitere kürzlich erschienene Publikation bestätigte die Vorteile einer frühzeitigen Parazentese bei Patienten mit Leberzirrhose und Aszites, die stationär aufgenommen werden. Eine Metaanalyse von Beobachtungsstudien (fast 80.000 Patienten mit Leberzirrhose und Aszites) zeigte, dass Patienten, bei denen innerhalb von 24 Stunden nach der Aufnahme eine diagnostische Parazentese durchgeführt wurde – im Vergleich zu Patienten mit verzögerter oder keiner Parazentese – signifikant seltener ein akutes Nierenversagen, eine kürzere Krankenhausverweildauer und eine geringere Krankenhaussterblichkeit (7 % vs. 10 %) aufwiesen. All diese Ergebnisse sprechen für eine frühzeitige diagnostische Parazentese bei Patienten mit Leberzirrhose und Aszites, die stationär behandelt werden müssen.
Eine abschließende Studie stellte die Annahme infrage, dass alle Patienten mit einer vorangegangenen Diagnose einer spontanen bakteriellen Peritonitis (SBP) eine dauerhafte Antibiotikaprophylaxe benötigen. In einer retrospektiven Analyse von über 11.000 Patienten mit SBP in der Vorgeschichte war ein Rezidiv zwei Jahre nach der SBP-Episode bei Patienten mit Antibiotikaprophylaxe signifikant häufiger als bei Patienten ohne (24 % vs. 15 %). Man vermutet, dass die jüngsten Veränderungen in der Mikrobiologie der SBP und die zunehmende Antibiotikaresistenz den potenziellen Nutzen einer chronischen Antibiotikaprophylaxe einschränken könnten.
FAZIT für die Praxis: Bei Patient:innen mit Zirrhose und beginnendem Aszites sollte ß-Blocker (vorzugsweise Carvedilol) so früh als möglich gegeben werden. Ebenso sollten auch geringere Aszitesmengen frühzeitig durch Paracentese abgelassen werden. Beide Maßnahmen haben einen hochsignifikanten Einfluss auf die 1-Jahres Morbidität und Mortalität. Eine dauerhafte Antibiotikaprophylaxe ist bei Patient:innen mit stattgehabter primärer spontaner Peritonitis in den meisten Fällen nicht angezeigt.
Literatur:
Übersetzung einer Zusammenfassung von Dressler DD. aus dem NEJM Clinician vom 30 Dez. 2025
GABAPENTIN ZUR SCHMERZREDUKTION NACH GROSSEN CHIRURGISCHEN EINGRIFFE
Gabapentin ist eine antikonvulsive Substanz, die zur Behandlung von neuropatischen Schmerzen und Epilepsie zugelassen ist. Gabapentin wird aber auch seit einigen Jahren als Teil einer multimodalen Schmerztherapie nach großen chirurgischen Eingriffen verabreicht, mit dem Ziel den opiatverbrauch zu verringern.
In einer doppelt-blinden, randomisierten Untersuchung wurden erwachsenen Patient:innen nach großen operativen Eingriffen (kardiale-, thorakale-, abdominelle OP´s) entweder 600mg Gabapentin präoperativ und 2x300mg postoperativ für 2 Tage oder eine Placebo zu gleichen Zeitpunkten verabreicht. Insgesamt wurden dazu 1196 Patient:innen (Medianalter 70 Jahre; zirka 76% Männer) randomisiert. Der primäre Outcomeparameter war die Hospitalsaufenthaltsdauer. Sekundäre Outcomeparameter waren Schmerzintensität, Opiatverbrauch, Nebenwirkungen und Lebensqualität unmittelbar nach dem Eingriff, sowie bis 4 Wochen und 4 Monate danach.
Der Zusatz von Gabapentin zur multimodalen Schmerztherapie nach großen operativen Eingriffen hatte keinen signifikanten Einfluss auf die Dauer des Hospitalaufenthaltes, dem kumulativen Opiatverbrauch, der Schmerzintensitäten nach dem Eingriff und der Lebensqualität. Die zusätzliche Gabe von Gabapentin führte allerdings zu einer höheren Inzidenz von chronischen Schmerzen nach 4 Monaten.
FAZIT für die Praxis: Wenn man die Studie genau liest, erkennt man, dass zwar der Opiatverbrauch in der Gabapentingruppe in den ersten 24h etwas geringer war – aber dieser Befund war nicht mit einer Reduktion von unerwünschten Nebenwirkungen verknüpft. Mehr Patient:innen in der Gabapentingruppe berichteten nach 4 Monaten über persistierende Schmerzen. Allerdings waren Schmerzintensitäten auch nach diesem Zeitraum ähnlich mit jenen in der Placebogruppe. Die letzte Metaanalyse zum Thema mit insgesamt 24682 Personen zeigte ebenfalls keinen klinisch relevanten Effekt auf die akute und chronische Schmerztherapie nach chirurgischen Eingriffen durch Gabapentoide. Aus diesen Gründen sollten Gabapentoide kein routinemäßiger Teil einer multimodalen postoperativen Schmerztherapie mehr sein!
Literatur:
Baos S, et al. Gabapentin for pain management after major surgery: a placebo-controlled, double-blinded, randomized clinical trial (the GAP study). Anesthesiology 2025; 143:851-861
Verret M, et al. Perioperative use of gabapentinoids for the management of postoperative acute pain: a systematic review and meta-analysis. Anaesthesiology 2020; 133: 265-279
SS-LAKTAM ANTIBIOTIKA PROPHYLAXE ZUR VERHINDERUNG VON CHIRURGISCHEN WUNDINFEKTIONE
ß-Laktam Antibiotika werden bei vielen chirurgischen Eingriffen in Orthopädie, Unfall- und Allgemeinchirurgie zur Prophylaxe von postoperativen Wundinfektionen verabreicht. Gelegentlich wird auf andere Antibiotika wie z.B. Clindamycin, Fluoroquinolone oder Vancomycin zurückgegriffen, obwohl mehrere Studien zeigen, dass nicht-ß Laktam Antibiotika schlechter als Prophylaxe für Wundinfektionen abschneiden.
In einer retrospektiven, nationalen Studie in der Schweiz mit 350.000 erwachsene Patient:innen wurden Effekte verschiedener präoperativ gegebener Antibiotika auf die Inzidenz postoperativer Wundinfektionen genauer untersucht. 98% aller Patient:innen erhielten ß-Laktame, der Rest andere Antibiotikaklassen.
Die Hauptresultate der Studie waren:
- Chirurgische Wundinfektionen waren doppelt so häufig bei Patient:innen, die nicht ß-Laktam Antibiotika erhielten (6,1% versus 2,8%) unabhängig davon welche Antibiotikaklassen verabreicht wurden! Die Unterschiede waren bei allen Typen von Wundinfekten (oberflächlich, tief, organbezogen) gleich ausgeprägt
- Betrachtet man die verwendeten nicht-ß Laktam Antibiotikaklassen wurden erhöhte Wundinfektionsraten in ähnlicher Inzidenz bei Verwendung von Clindamycin, Vancomycin und Ciprofloxacin beobachtet.
FAZIT für die Praxis: Eine Prophylaxe mit nicht ß-Laktam Antibiotika wird meist bei Patient:innen mit bekannter oder Verdacht auf Penicillinallergie (PNC-Allergie) verabreicht oder, wenn Bedenken hinsichtlich einer möglichen Hautbesiedelung mit einem multiresistenten Staphylokkokus aureus bestehen. Cefazolin hat im Unterschied zu nicht-ß-Laktam Antibiotika ein extrem niedriges Risiko für allergische IgE vermittelte Reaktionen und Kreuzallergien zwischen Penicillinen und Cephalosporinen sind sehr selten. Deshalb wird eine chirurgische Infektionsprophylaxe mit Cephazolin auch bei vorbestehender Penicillinallergie in den meisten Fällen empfohlen. Bei Patient:innen mit Verdacht auf MRSA Besiedelung empfehlen einige Autoren sogar eine „doppelte“ Antibiotikaprophylaxe mit Vancomycin und einem ß-Laktam vor einem chirurgischen Eingriff.
Wir gehen in der Praxis folgendermaßen vor: Bei Patient:innen mit angeblicher oder bekannter PNC Allergie ohne schwerer kardiorespiratorischer Symptomatik verwenden wir Cephalosporine zur Infektionsprophylaxe. Bei Patient:innen mit einer schweren Reaktion auf Penicilline (allergischen Schockgeschehen) weichen wir auf Alternativantibiotika aus (Chinolone oder Vancomycin). Selbstverständlich ist die ausreichende Dosierung und das Timing ein wesentlicher Erfolgsfaktor der Infektionsprophylaxe – nur, wenn vor dem Hautschnitt ausreichende Gewebespiegel des Antibiotikums in der Subkutis vorliegen, kann ein Abtöten von Hautkeimen gewährleistet werden. Deshalb soll die Antibiotikaprophylaxe mindestens 10-20 Minuten vor dem Hautschnitt verabreicht werden. Bei übergewichtigen Patient:innen geben wir initial eine doppelte Standarddosis (z.B. Curocef 3g oder Tazonam 9/1g iv). Dauert der Eingriff lange, sollte die Antibiotikagabe spätestens nach ca. 2 Halbwertszeiten, in Standarddosierung, wiederholt werden.
Literatur:
Largiader S, et al. ß-lactam vs non-ßlactam antimicrobial prophylaxis and surgical site infection. JAMA Netw Open 2025;8: e250809
PRO UND CON BESONDERER KONTAKTBESCHRÄNKUNGEN BEI PATIENT:INNEN MIT MRSA (MULTIRESISTENTER STAPHYLOKOKKUS AUREUS) ODER VRE (VANCOMYCIN RESISTENTER ENTEROKOKKUS )NACHWEIS
Die folgenden Texte von Sara M. Karaba, M.D., Ph.D., M.H.S. und Anne-Catrin Uhlemann, M.D., Ph.D.
habe ich mit minimalen Kürzungen aus dem NEJM im Orginaltext übernommen. Die Diskussion über Kontaktbeschränkungen bei Patient:innen mit MRSA oder VRE Besiedelung läuft seit zirka 10 Jahren und die kontroversen Meinungen sind durch gute Argumente untermauert!
Empfehlung zur Fortsetzung der Kontaktvorkehrungen
Sara M. Karaba, M.D., Ph.D., M.H.S.
Multiresistente Erreger verursachen weltweit erhebliche Morbidität und Mortalität, und die Centers for Disease Control and Prevention (CDC) stufen MRSA und VRE als ernstzunehmende Bedrohungen ein. Im Jahr 2017 gab es in den Vereinigten Staaten mehr als 300.000 Fälle von MRSA- und VRE-Infektionen bei stationären Patienten, die zu 16.000 Todesfällen und Gesundheitskosten von über 2 Milliarden US-Dollar führten. Da klinische Umgebungen und medizinisches Personal nachweislich schnell mit VRE oder MRSA von kolonisierten oder infizierten Patienten kontaminiert werden, werden Kontaktvorkehrungen – die Verwendung von Schutzkittel und Handschuhen nach der Händedesinfektion – empfohlen, um die Übertragung dieser Erreger im Krankenhaus zu unterbrechen. Die BUGG-Studie (Benefits of Universal Glove and Gown) untersuchte die Anwendung universeller Kontaktvorkehrungen (für alle Patienten auf der Intensivstation, unabhängig vom Kolonisationsstatus) und zeigte, dass diese mit einem signifikant geringeren Risiko einer MRSA-Infektion (einem wichtigen sekundären Endpunkt) verbunden waren. Der Ansatz deutete auch auf eine nicht signifikante Verringerung der MRSA- oder VRE-Infektion (dem primären Endpunkt) und unerwünschter Ereignisse hin. Das US-Veteranenministerium (VA) implementierte ein Infektionspräventionspaket, das Kontaktvorkehrungen für Patienten mit MRSA-Kolonisation oder -Infektion umfasste, und beobachtete in den folgenden zehn Jahren einen Rückgang der im Krankenhaus erworbenen MRSA-Infektionen um 66 %. Allerdings werden Kontaktvorkehrungen häufig zusammen mit anderen Infektionspräventionsstrategien untersucht, darunter Händedesinfektion, Umgebungsreinigung und Chlorhexidin-Desinfektion. Gluconatbäder und der rationale Einsatz von Antibiotika erschweren es, die Wirksamkeit der Kontaktvorkehrungen allein zu beurteilen. Obwohl einige Studien keinen Anstieg nosokomialer Infektionen nach dem Absetzen von Kontaktvorkehrungen gegen MRSA oder VRE zeigten, schränken methodische Bedenken deren Interpretation und Generalisierbarkeit ein. Mehrere Studien untersuchten die MRSA-Neuinfektion nicht als Endpunkt, und keine untersuchte Infektionen nach nosokomialer MRSA-Kolonisation. Es gibt Hinweise darauf, dass über 60 % der MRSA-Infektionen nach der Krankenhausentlassung auftreten und dass bei MRSA-kolonisierten Patienten sowohl vor als auch nach der Entlassung ein erhöhtes Infektionsrisiko besteht. Im Fall von VRE zeigten einige Studien keinen Effekt auf nosokomiale Infektionen nach Aufhebung der Kontaktisolierung. Eine Studie wies jedoch einen deutlichen und anhaltenden Anstieg von VRE-Blutstrominfektionen nach, der mit dem Ende der Kontaktisolierung bei Patienten mit VRE-Infektion oder -Kolonisation in mehreren Krankenhäusern einherging. Ein potenzieller Nachteil der Kontaktisolierung ist das Risiko von Depressionen, Angstzuständen und Unzufriedenheit sowie eines Sturzrisikos bei Patienten, die unter Kontaktisolierung behandelt werden. Studien, die den Schweregrad der Erkrankung und Depressionen berücksichtigten, zeigten jedoch keinen solchen Zusammenhang. In der randomisierten BUGG-Studie war die Rate unerwünschter Ereignisse auf Intensivstationen, die universelle Kontaktvorkehrungen umsetzten, nicht signifikant niedriger als auf solchen, die dies nicht taten. Kontaktvorkehrungen sind ein wichtiges Instrument zur Verhinderung der Übertragung und des Erwerbs multiresistenter Erreger, einschließlich MRSA und VRE. Die Anwendung von Kontaktvorkehrungen sollte bei Patienten mit MRSA- oder VRE-Kolonisation oder -Infektion fortgesetzt werden.
Empfehlung zur Beendigung von Kontaktisolierungsmaßnahmen
Anne-Catrin Uhlemann, M.D., Ph.D.
Der Nutzen von Kontaktisolierungsmaßnahmen bei Patienten mit MRSA- oder VRE-Infektion bzw. -Kolonisation ist Gegenstand hitziger Debatten. Nicht nur konnten zahlreiche Studien, darunter auch Cluster-randomisierte Studien, die Wirksamkeit von Kontaktisolierungsmaßnahmen zur Reduzierung der MRSA- und VRE-Infektionen nicht belegen, auch eine zunehmende Anzahl quasi-experimenteller Studien und Metaanalysen hat gezeigt, dass die Beendigung von Kontaktisolierungsmaßnahmen nicht zu einem Anstieg nosokomialer MRSA-Infektionen geführt hat.
Die Isolierung von Patienten mit Infektionen oder Kolonisationen durch multiresistente Erreger wie MRSA und VRE sowie die Anwendung von Kontaktvorkehrungen waren Mitte der 1990er-Jahre sinnvoll, da die Antibiotikaauswahl begrenzt war und die Entwicklung von Vancomycin-Resistenzen bei MRSA möglich schien. Seitdem hat sich vieles verändert. Trotz der weitverbreiteten Anwendung für Patienten mit MRSA- oder VRE-Infektionen oder -Kolonisationen sind diese Erreger endemisch und weiterhin häufige Ursachen für Krankenhausinfektionen. Darüber hinaus hat sich die Epidemiologie von MRSA deutlich verändert. MRSA ist nicht auf Krankenhäuser beschränkt; Patienten können auch außerhalb von Krankenhäusern kolonisiert sein. Erfreulicherweise hat sich die befürchtete Vancomycin-Resistenz bei MRSA jedoch nicht bewahrheitet, und es stehen mittlerweile viele neue, wirksame Antibiotika zur Verfügung. Darüber hinaus hat die Sequenzierung bakterieller Genome, die eine präzise Nachverfolgung der Erregerübertragung ermöglicht, gezeigt, dass die Übertragung von Patient zu Patient nur einen kleinen Teil der MRSA-Infektionen im Krankenhaus ausmacht, auch solche, die nach Aufhebung der Kontaktisolierung auftreten. Es ist wichtig zu beachten, dass das Screening von Patienten auf MRSA und VRE und die damit verbundene Kontaktisolierung erhebliche Einschränkungen für die betroffenen Patienten mit sich bringt, ohne dass ein Nutzen für andere vermutet wird. Die unbeabsichtigten negativen Folgen der Kontaktisolierung für Patienten mit MRSA- oder VRE-Kolonisation sind nicht zu unterschätzen. Dazu gehört eine verminderte Interaktion mit medizinischem Fachpersonal, verstärkte soziale Isolation und höhere Raten von Angstzuständen und Depressionen. Diese negativen Folgen werden verstärkt, wenn die Kontaktisolierung die Unterbringung von Patienten in Einzelzimmern erfordert. Dies kann den Patientenfluss beeinträchtigen, zu Verzögerungen in der Versorgung kolonisierter Patienten führen, wenn keine Einzelzimmer verfügbar sind, und die Nutzung dieser Zimmer für Patienten verhindern, die sie dringend benötigen. Darüber hinaus führen Kontaktvorkehrungen zu enormen Abfallmengen und Treibhausgasemissionen durch die Entsorgung von Einweg-Isolationskitteln und Nitrilhandschuhen. Schätzungen zufolge verbraucht das US-amerikanische Gesundheitssystem allein für MRSA-Kontaktvorkehrungen jährlich etwa 1,5 Milliarden Kittel und Handschuhe, was einem Abfallaufkommen von 66 Millionen Pfund und Kosten von 1,87 Milliarden US-Dollar entspricht. Der Einsatz universeller Kontaktvorkehrungen für Patienten mit MRSA- oder VRE-Infektion oder -Kolonisation sollte eingestellt werden. Dies liegt an fehlenden überzeugenden Belegen dafür, dass diese Praxis Krankenhausinfektionen und die Übertragung dieser Erreger reduziert, an den möglichen Schäden für Patienten sowie an den erheblichen Umwelt- und Finanzkosten. Der Fokus sollte verstärkt auf die Verbesserung der Händehygiene, den gezielten Einsatz von Kontaktvorkehrungen in Hochrisikosituationen und Dekolonisierungsmaßnahmen wie Chlorhexidinbäder gelegt werden.
FAZIT für die Praxis: Ich denke, dass ein Mittelweg aus beiden Argumentationssträngen in der klinischen Praxis sinnvoll ist. Wir verzichten auf Einzelzimmerisolation derartiger Patienten, nutzen aber, neben dem Einhalten der üblichen Hygienemaßnahmen, das Tragen von Einmalhandschuhen und einer Einmalschürze bei jedem direkten Patient:innenkontakt. Die Inzidenz von MRSA und VRE ist österreichweit extrem unterschiedlich! Wir haben das Glück, dass diese Isolate bei unseren Patient:innen noch eher selten gefunden werden.
Literatur:
Sara M. Karaba und Anne-Catrin Uhlemann. Contact precautions for MRSA and Vanvomycin-Resistant Enterococcus. NEJM 2025; 393: 2475-2477
COVID IN DER SCHWANGERSCHAFT – HILFT DIE IMPFUNG?
Im Jahr 2025 hat die CDC ihre Impfempfehlungen bezüglich COVID-19 für schwangere oder stillende Mütter aufgehoben. Andere medizinische Gesellschaften und behörden empfehlen die Impfung mit Nachdruck weiter. Eine neue Studie zeigt deutlich die positiven Wirkungen einer COVID-19 Impfung auf das mütterliche und perinatale Outcome:
Mithilfe einer kanadischen Datenbank konnten die Autoren insgesamt 20.000 Schwangerschaften identifizieren, von denen 72% geimpft waren und bei denen eine COVID-19 Diagnose zwischen April 2012 und Dezember 2022 (Delta und Omikron Varianten) gestellt wurde.
Hauptresultate:
- In der Delta Varianten Periode mussten 13,5% der ungeimpften Schwangeren, wegen schwere Symptomatik, in einem Krankenhaus aufgenommen werden. Im Gegensatz dazu wurden nur 4,8% der Geimpften hospitalisiert! 4,8% der Ungeimpften mussten auf Intensivstationen behandelt werden, während nur 0,3% der Geimpften intensivmedizinisch behandelt wurden
- In der Omikron Periode wurden 5,3% der ungeimpften Schwangeren in einem Krankenhaus aufgenommen werden, aber nur 1,5% der Geimpften hospitalisiert! 1% der Ungeimpften mussten auf Intensivstationen behandelt werden, während nur 0,05% der Geimpften intensivmedizinisch behandelt wurden
- Diese Ergebnisse waren in beiden Perioden unabhängig von Vorhandensein definierter Vorerkrankungen und sozialer Unterschiede
- Nichtgeimpfte schwangere hatten signifikant häufigere Frühgeburten (9,6%) im Vergleich mit Geimpften (7,2%)
FAZIT für die Praxis: Die COVID-19 Impfung ist nicht nur sicher sondern sie senkt die maternale und kindliche Morbidität!
Literatur:McClymont E. The role of vaccination in maternal and perinatal outcomes associated with COVID-19 in pregnancy. JAMA 2025; doi: 10.1001/jama.2025.21001
